А.А. Суханова, Н.Я. Ратушняк, О.А. Сорокина
Украинский государственный институт репродуктологии Национальной медицинской академии последипломного образования имени П.Л. Шупика,
г. Киев
В статье освещен современный взгляд на процесс формирования, лечения и профилактики перитонеальных тазовых спаек. Известно, что спаечная болезнь увеличивает риск возникновения кишечной непроходимости, бесплодия, хронической тазовой боли и хирургических осложнений, поэтому целью исследования является создание алгоритма профилактики спаечной болезни у пациенток в раннем послеоперационном периоде
Ключевые слова: тазовые спайки, гинекология, хирургия, лапаротомия, лапароскопия.
Спаечная болезнь малого таза – проблема оперативной гинекологии, известная врачам со времен Гиппократа. Первые описания спаечного процесса датируются XVI веком (Vesarius A De Corporis Humani Fabrica In., 1543). Упоминания спаечной болезни в документальных материалах начинается с публикации Hunter (1793).
Проблема спаечной болезни актуальна до сих пор. Согласно классификации ВОЗ, принятой в 1990 году в Женеве Всемирной Ассамблеей Здравоохранения (Международная классификация болезней 10-го просмотра), тазовые спайки у женщин выделены в отдельный раздел.
Ведущими факторами, которые обусловливают образование спаек в малом тазу, являются операции на органах брюшной полости и малого таза (лапаротомия, лапароскопия), воспалительные заболевания придатков матки и наружный генитальный эндометриоз.
По данным исследования SURGERY AND CLINICAL ADHESIONS RESEARCH в Швейцарии: у 30% пациенток, перенесших операции на органах брюшной полости и малого таза, в течение 10 последующих лет возникают клинические проявления спаек, из них в течение первого года госпитализируют 20% пациенток, среди которых 4,5% – по поводу тонкокишечной непроходимости. Наиболее часто спайки, приводящие к госпитализации, возникают после оперативных вмешательств в абдоминальной хирургии и гинекологии.
Нерешенными остаются вопросы патогенеза, профилактики и лечения спаечного процесса. Известно, что пусковыми механизмами в образовании спаек являются следующие факторы:
- механический – травматизация брюшины в ходе рассечения, захвата инструментами, промокание и протирание сухими марлевыми салфетками, иссечение участков брюшины в процессе хирургического вмешательства;
- физический – высушивание брюшины воздухом, действие высокой температуры (ожоги) при использовании во время операции электроножа, лазерного излучения, горячих растворов;
- инфекционный – попадание инфекции в брюшную полость эндогенным (воспалительный процесс органов брюшной полости с развитием местного и общего воспаления брюшины) и экзогенным (при ранении, перфорации полого органа) путями;
- имплантационный – асептическое воспаление брюшины вследствие оставления в брюшной полости тампонов, дренажных трубок, нерассасывающегося или рассасывающегося длительное время шовного материала, лоскутов марли, талька из перчаток, кровоизлияний и гематом брюшины;
- химический – попадание во время операции в брюшную полость веществ, вызывающих химический ожог и асептическое воспаление брюшины (йод, спирт, концентрированные растворы антибиотиков и т.п.).
Формирование спаек – это нарушение баланса между ангиогенными, фибриногенными и фибринолитическими факторами.
Несмотря на разнообразие причин, обуславливающих развитие спаечного процесса в малом тазу, главные цели поиска направлены на изучение этиологии и профилактики именно послеоперационных тазовых спаек.
Результаты экспериментальных исследований позволяют выделить 5 фаз адгезиогенеза при повреждении брюшины:
- Реактивная фаза (первые 12 ч) клинически и морфологически проявляется признаками шока, определяется повреждение брюшины.
- Фаза экссудации (1–3-е сутки). Процессы экссудации преобладают над сопутствующими процессами воспаления. Повышается проницаемость сосудистого русла, что приводит к выходу в свободную брюшную полость перитонеальных малодифференцированных полипотентных клеток, клеток воспаления и жидкой части крови, которая содержит фибриноген.
- Фаза адгезии (3-е сутки). Отложение фибрина на поврежденных поверхностях, склеивание их. Полипотентные клетки брюшинного экссудата дифференцируются в фибробласты, продуцирующие коллаген.
- Фаза молодых сращений (7–14-е сутки). Образуются рыхлые спайки, содержащие недостаточное количество коллагена. В спайках происходит образование новых сосудов и миграция гладкомышечных клеток.
Повышенная склонность к развитию спаек в брюшной полости связана с конституциональными особенностями организма.
Для лечения спаечной болезни используют консервативный или оперативный метод. Показаниями к операции являются: острый приступ спаечной непроходимости кишечника, рецидивирующее течение спаечной болезни. В гинекологии, основным методом хирургического лечения спаечной болезни является лапароскопический адгезиолизис.
На сегодняшний день предложено немало технических приемов и препаратов, предупреждающих образование послеоперационных спаек. Основные подходы к профилактике спаечной болезни заключаются в следующем:
- своевременное оперативное вмешательство;
- промывание брюшной полости;
- антибиотикотерапия;
- применение антикоагулянтов;
- стимуляция моторики кишечника;
- использование протеолитических и фибринолитических ферментов;
- оснащение инсуфлятора кондиционером.
Цель исследования: профилактика образования спаек у больных в послеоперационном периоде.
МАТЕРИАЛЫ И МЕТОДЫ
Исследование выполнено на базе КГЦРПМ с января 2017 по июнь 2018 года.
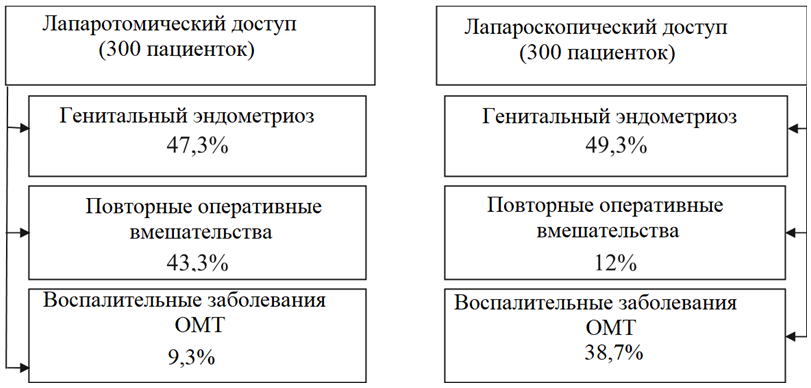
Рис. 1. Распределение больных со спаечной болезнью в зависимости от вида и показаний к оперативному вмешательству.
Исследование проводилось в два этапа.
На первом этапе было проведено ретроспективный анализ амбулаторных карт 1500 пациенток в возрасте от 20 до 65 лет, которым выполняли оперативное лечение гинекологических заболеваний лапаротомическим и лапароскопическим оперативными доступами.
Среди пациенток, у которых интраоперационно был выявлен спаечный процесс органов малого таза (ОМТ), проанализированы клинико-анамнестические данные. Особое внимание обращалось на наличие генитального эндометриоза, повторные оперативные вмешательства и хронические воспалительные процессы.
На втором этапе пациенток разделили на две группы: I группа (основная) и II группа (контрольная).
В I группу (основную) было включено 86 пациенток, которые в послеоперационном периоде получали стандартную схему лечения и препараты тиотриазолина (Далмаксин) по 1 суппозиторию ректально с 1 дня после операции на протяжении 14 дней (конец фазы молодых сращений в процессе образования спаек).
Во ІІ группу (контрольную) были включены 73 пациентки в послеоперационном периоде, получавшие стандартную схему лечения.
Противовоспалительный эффект, как результат ингибирования перекисного окисления липидов в травмированных тканях, позволяет усилить действие НПВС и быстрее избавиться от болевого синдрома.
Сокращение периода воспаления в значительной мере происходит за счет сокращения длительности фазы альтерации, первого этапа воспаления, который, главным образом, и обуславливает дальнейшие последствия процесса.
Также обращают на себя внимание мягкие фибринолитические свойства тиотриазолина, которые лучше всего реализуются в условиях оксидантного стресса в поврежденных вмешательством тканях, за счет усиления компенсаторной активации анаэробного гликолиза и активации процессов окисления в цикле Кребса с сохранением внутриклеточного фонда АТФ.
Тиотриазолин, особенно в условиях ишемической патологии, проявляет умеренную фибринолитическую активность и способствует повышению активности фибринолиза. При этом, прямого фибринолитического воздействия препарат не оказывает, основной эффект реализуется благодаря выраженному антиоксидантному действию, а именно – связыванию активных форм кислорода (АФК) и модуляции экспрессии тканевого плазминогена. Таким образом, тиотриазолин проявляет умеренные фибринолитические свойства непосредственно при возникновении патологических явлений на фоне активации оксидантного стресса. В отличие от классических фибринолитиков и антикоагулянтов, тиотриазолин не способен вызвать кровотечение или антиген-обусловленный тромбоз. Полная безопасность тиотриазолина в отношении гемостаза подтверждена многочисленными клиническими исследованиями в отечественных и зарубежных учреждениях. Ни в одном из них не было зарегистрировано случаев послеоперационного кровотечения или возникновения некомпетентности швов.
Этим тиотриазолин фундаментально отличается от препаратов протеолитических ферментов (стрептокиназа, стрептодорназа), которые растворяют любые отложения фибрина и поэтому, из-за риска кровотечения из вовлеченных в операцию участков тела, не могут применяться в первые дни после вмешательства. Назначение «Далмаксина» с первых суток после операции минимизирует проявления наиболее важных в развитии спаек фаз: реактивной и экссудативной.
Под влиянием тиотриазолина нарушается основной фактор воспаления, а именно – переход клеточного обмена в условиях ишемии на альтернативный, анаэробный механизм. В условиях дефицита активного кислорода в клетках накапливаются продукты анаэробного гликолиза (лактат) и смещается рН в сторону закисления. Как следствие, повышается проницаемость клеточных мембран, что может привести к разрушению клетки.
Противоишемическое и противовоспалительное действие тиатриазолина заключается в сохранении и увеличении внутриклеточных запасов АТФ. Как следствие, метаболизм возвращается к продуктивному аэробному механизму, нормализуется pH. А уже за счет этого значительно уменьшается массивность пропотевания фибриногена и полипотентных клеток в брюшной полости, отсюда – исчезает сама основа для образования спаек брюшины и развития спаечной болезни в отдаленном периоде.
Таким образом, тиатриазолин уменьшает риск метаболического ацидоза, нормализует pH и способствует снижению экспрессии ключевых факторов развития спаечного процесса.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
На первом этапе исследования было обнаружено, что из 1500 пациенток, у 1230 (82%) имеется спаечная болезнь, соответственно у 270 (18%) пациенток, спаечный процесс отсутствовал.
Пациенток, у которых была обнаружена спаечная болезнь (600 человек), распределили на две группы в зависимости от вида оперативного вмешательства. Целью этого анализа было выявление основных этиологических факторов развития спаечного процесса ОМТ и определение влияния вида оперативного вмешательства (рисунок).
Согласно полученным данным, генитальный эндометриоз – это основной этиологический фактор спаечного процесса ОМТ у 47,3% пациенток при лапаратомическом вмешательстве и у 49,3% – при лапараскопическом. Количество повторных оперативных вмешательств в анамнезе преобладает в группе пациенток с лапаротомическим доступом – 43,3%, при лапароскопии повторные вмешательства были у 12%. Но, учитывая данные многих исследований, сделан вывод, что лапароскопическая хирургия незначительно уменьшает распространенность и степень вовлечения кишечника в спаечный процесс. Возможно, снижает распространенность спаек непосредственно в зоне оперативного вмешательства, однако не приводит к профилактике спаек, поскольку не уменьшает спайкообразование в контексте патогенеза этого процесса. Следовательно, лапароскопическая хирургия практически не снижает частоты распространенности спаечного процесса.
Таблица 1 Результаты лечения больных I и II групп в послеоперационном периоде
| Показатель | І группа, n=86 | ІІ группа, n=73 | р |
| Период гиперемии, дней | 0,91±0,22 | 2,71±0,57 | 0,008 |
| Количество пациенток с гипертермией дольше 3 дней, n (%) | 6 (6,9) | 14 (19,2) | 0,047 |
| Средняя длительность пребывания в стационаре, дней | 2,2±1,1 | 3,3±0,7 | 0,002 |
Анамнестически, воспалительные заболевания ОМТ преобладают в группе с лапароскопическим доступом – 38,7%, при лапаратомии 9,3%.
На следующем этапе исследования оценивали течение послеоперационного периода у пациенток, разделенных на две группы. В I группу (основную) вошли 86 женщин, получавших стандартную схему лечения, которая предусматривала использование антибактериальной, противовоспалительной, обезболивающей и симптоматической терапии и тиатриазолин (Далмаксин) по 1 суппозиторию ректально 1 раз в сутки в течение 14 дней до окончания фазы молодых сращений. Во ІІ группу (контрольную) вошли 73 женщины, которым в послеоперационном периоде была назначена стандартная схема лечения.
Согласно полученным результатам, отраженным в таблице, период гиперемии во II группе длился в 2 раза дольше, чем в I группе. Также II группа преобладает по количеству пациентов с гипертермией более 3 суток – 14 (19,2%) в сравнении с I группой – 6 (6,9%) пациенток. По времени пребывания в стационаре снова преобладает II группа (контрольная) – 3,3%, которая получала стандартную схему лечения в послеоперационном периоде в сравнении с I группой (основной) – 2,2%.
Течение раннего послеоперационного периода оценивали исходя из оценки болевого синдрома по десятибалльной шкале, наличию осложнений.
Прооперированные пациентки из I (основной) группы, оценивали послеоперационный болевой синдром в среднем в 3,1 балла (p=0,00), из ІІ группы (контрольной) – в 3,4 балла (p=0,06).
Для обезболивания использовались синтетические опиоидные анальгетики и нестероидные противовоспалительные средства, которые вводили внутримышечно.
Оперированным с II группы потребовалось большее количество инъекций препаратов обеих групп в расчете на одну больную (5±3 и 6±1, 9±5 и 14±4 соответственно). Разница была статистически достоверной (р=0,009 и р=0,006).
ВЫВОДЫ
Спаечная болезнь оказывает негативное влияние на состояние здоровья больных, увеличивая риск возникновения кишечной непроходимости, бесплодия, хронической тазовой боли и хирургических осложнений, связанных с интраоперационной травматизацией внутренних органов.
Необходимо своевременно выделять среди пациентов группу риска развития спаечного процесса в послеоперационном периоде.
Раннее начало профилактики спаечного процесса с применением тиотриазолина (Далмаксина) в дополнение к стандартной схеме лечения этиопатогенетически обосновано, улучшает течение послеоперационного периода и предупреждает развитие спаечного процесса.
Патогенетические подходы к профилактике перитонеальных тазовых спаек А.А. Суханова, Н.Я. Ратушняк, О.А. Сорокина
В статье освещен современный взгляд на процесс образования, лечения и профилактики перитонеальных тазовых спаек. Известно, что спаечная болезнь увеличивает риск возникновения кишечной непроходимости, бесплодия, хронической тазовой боли и хирургических осложнений, поэтому целью данного исследования является создание алгоритма профилактики возникновения спаечной болезни у пациенток в ранний послеоперационный период.
Ключевые слова: тазовые спайки, гинекология, хирургия, лапаротомия, лапароскопия.
Pathogenetic approaches to the prevention of peritoneal pelvic adhesions
A.A. Sukhanova, N.Ya. Ratushnyak, O.A. Sorokina
The article highlights the modern view on the process of education, treatment and prevention of peritoneal pelvic adhesions. It is known that adhesive disease increases the risk of intestinal obstruction, infertility, chronic pelvic pain and surgical complications, therefore the purpose of this study is to create an algorithm for preventing the occurrence of adhesive disease in patients in the early postoperative period.
Key words: pelvic adhesions, gynecology, surgery, laparotomy, laparoscopy.
Сведения об авторах
Суханова Аурика Альбертовна – Кафедра акушерства, гинекологии и репродуктологии Украинского государственного института репродуктологии Национальной медицинской академии последипломного образования имени П.Л. Шупика. 01011, г. Киев, ул. Арсенальная, 5. E-mail: a.sukhanova@gmail.com
Ратушняк Наталья Ярославовна – Кафедра акушерства, гинекологии и репродуктологии Украинского государственного института репродуктологии Национальной медицинской академии последипломного образования имени П.Л. Шупика. 01011, г. Киев, ул. Арсенальная, 5.
Сорокина Оксана Александровна – Кафедра акушерства, гинекологии и репродуктологии Украинского государственного института репродуктологии Национальной медицинской академии последипломного образования имени П.Л. Шупика. 01011, г. Киев, ул. Арсенальная, 5.
СПИСОК ЛИТЕРАТУРЫ
- Аюшинова Н.И., Лепехова С.А., Шурыгина И.А. и др. Способ моделирования спаечного процесса в брюшной полости // Патент на изобретение RUS 2467401 27.07.2011.
- Бебуришвили А.Г., Воробьев А.А., Михин И.В. и др. Спаечная болезнь брюшной полости //Эндоскопическая хирургия. – 2003. – № 1. – С. 51–62.
- Беженарь В.Ф., Байлюк Е.Н., Цыпурдеева А.А. Клиническое значение противоспаечных барьеров в профилактике образования спаек у гинекологических больных // Журнал акушерства и женских болезней. – 2009. – Т. LVIII. – Вып. 5:М3.
- Бурлев В.А., Дубинская Е.Д., Гаспаров А.С. Перитонеальные спайки: от патогенеза до профилактики // Проблемы репродукции. – 2009. – № 3. – С. 36–44.
- Верхулецкий И.Е., Верхулецкий Е.И. Аспекты морфологии и классификации спаечного процесса органов брюшной полости // Украинский журнал хирургии. – 2009. – № 3. – С. 30–33.
- Кулаков В.И., Адамян Л.В., Мынбаев О.А. Послеоперационные спайки (этиология, патогенез и профилактика). – М: Медицина, 1998. – 528 с.
- Матвеев Н.Л., Арутюнян Д.Ю. Внутрибрюшные спайки – недооцениваемая проблема (обзор литературы) // Эндоскопическая хирургия. – 2007. – T. 13, № 5. – С. 60–69.
- Попов А.А., Мананникова Т.Н., Шагинян Г.Г. Спаечная болезнь как проблема репродукции и методы ее профилактики // Российский вестник акушера-гинеколога. – 2005. – № 4. – С. 41–45.
- Серов В.В. Воспаление. Руководство для врачей / Под ред. В.В. Серова, В.С. Паукова. – М.: Медицина, 1995. – 219 с.
- Хусаинова В.Х., Федорова Т.А., Волков Н.И. Диагностика, лечение и профилактика спаечного процесса в малом тазу у женщин с трубно-перитонеальной формой бесплодия // Гинекология. – 2003. – Т. 5, № 2. – С. 117–122.
- Чекмазов И.А. Спаечная болезнь органов брюшной полости (патогенез, клиника, диагностика, лечение и профилактика): Дис. … д-ра мед. наук: 14.00.47 / Чекмазов И.А. [Место защиты: Центральный научно-исследовательский институт гастроэнтерологии]. – М., 2004. – 195 с.
- Мамчур В.И. Два препарата, один организм – механизмы взаимодействий при коморбидной патологии //Фармакология и лекарственная токсикология. – 2013. – № 6 (36). – С. 27–55.
- Di Zerega G.S., Campeau J.D. Peritoneal repair and post-surgical adhesion formation // Human reproduction update. – 2001. – № 6. – Vol. 6. – Р. 547–555.
- Gutt et al. Fewer adhesions induced by laparoscopic surgery? // Surg. Endosc. – 2004. – 18. – Р. 898–906.
- Kuhry E. et al. Long-term outcome of laparoscopic surgery for colorectal cancer: a cochrane systematic review of randomised controlled trials // Cancer Treat Rev. – 2008. – Oct; 34(6). – Р. 498–504.
- Lundorff et al. Adhesion formation after laparoscopic surgery in tubal pregnancy: a randomized trial versus laparotomy // Fertil Steril. – 1991. – 55 (5). – Р. 911–915.
- De Cherney A.H., di Zerega G.S. «Clinical problem of intraperitoneal postsurgical adhesion formation following general surgery and the use of adhesion prevention barriers.» Surg Clin North Am,77(1997):671-688.
- Stricker B., Blanco J., Fox H.E. «The gynecologic contribution to intestinal obstruction in females.» J Am Coll Surg,178(1994):617-620.
- Drollette C.M., Badawy S.Z. Pathophysiology of pelvic adhesions: Modern trends in preventing infertility // J. Reprod. Med. – 1992. – № 3. – P. 107–122.
- Ellis H. The clinical significance of adhesions: Focus on intestinal obstruction // Eur. J. Surg. Suppl. – 1997. – № 577. – Р. 5–9.
- Lalountas M.A., Ballas K.D., Skouras C., et al. Preventing intraperitoneal adhesions with atorvastatin and sodium hyaluronate/carboxymethylcellulose: a comparative study in rats // Am. J. Surg. – 2010. – Vol. 200. – № 1. – P. 118– 112.
- Whang S.H., Astudillo J.A., Sporn E., et al. In search of the best peritoneal adhesion model: comparison of different techniques in a rat model // J. Surg. Res. – 2011. – Vol. 167, № 2. – P. 245–25.
Share the post "Патогенетические подходы к профилактике перитонеальных тазовых спаек"

